

【好药记】一致性评价受理号突破600,299个为289品种;本周科伦20亿大品种,复星首家...
截止12月13日,CDE受理一致性评价申请受理号达616个(按补充申请计算,下同),涉及235家企业的217个品种药品;其中289目录药品受理号有299个(82个品种);已有98个受理号46个品种通过一致性评价,289品种仅22个通过一致性评价。本周(12月6日至12月13日)又有2个289目录药品过评,3个药品审批完毕,通过在即,还有36受理号23品种获承办,更多详情且随小编一起看看。
一致性评价办理状态更新
本周,重庆药友289目录药品氯化钾颗粒抢在大限之期前首家通过一致性评价,四川科伦的289品种阿莫西林胶囊(0.25g(按C16H19N3O5S计))通过一致性评价,成为该品种该规格第4家过评企业;此外,还有3品种“审批完毕-待制证”,通过在即,恒瑞两款重磅注射剂在内,为多西他赛注射液和盐酸伊立替康注射液,详情可见下表。
本周一致性评价审评审批办理详情

阿莫西林胶囊
12月13日,湖南科伦药业申报的阿莫西林胶囊通过一致性评价,阿莫西林胶囊为289目录品种,是医保甲类及2018版基药目录药品,2017年阿莫西林胶囊中国销售额约20.59亿元。据药智数据,其一致性评价申报非常火热,有19家企业申报,受理号达26个,目前加上科伦,通过企业达4家。
阿莫西林胶囊胶囊一致性评价通过详情
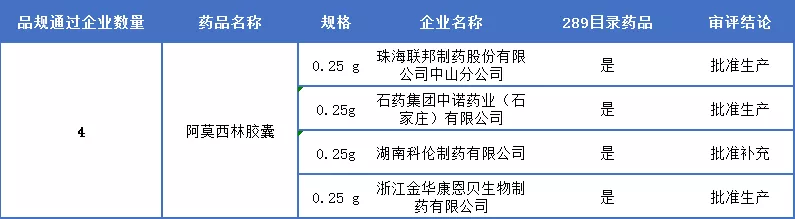
氯化钾颗粒
12月5日,复星医药其子公司重庆药友的289目录药品氯化钾颗粒首家通过一致性评价。据复星医药公告显示,2017年度,重庆药友该药品于中国境内(不包括港澳2台地区)销售额约为人民币71万元(未经审计)。截止10月,复星集团针对该药品一致性评价已投入研发费用人民币约154万元(未经审计)。
氯化钾颗粒主要治疗低钾血症、预防低钾血症,并适用于洋地黄中毒引起频发性、多源性早搏或快速心律失常。
据药智国产药品数据库,国产氯化钾颗粒生产单位仅3家,为武汉太福制药、重庆药友、杏辉天力(杭州)药业,目前仅重庆药友首家申报且首家过评。另外国内氯化钾制剂除了颗粒剂型还有90家企业持有氯化钾注射液生产批文,10家企业持有氯化钾缓释片生产批文,13家企业持有氯化钾片生产批文。
多西他赛注射液
12月10日,据药智药品注册与受理数据库显示,江苏恒瑞医药的多西他赛注射液其中1个受理号一致性评价“审批完毕-待制证”。
多西他赛是紫杉烷的半合成产物,是一种作用于细胞微管的抗癌药物,主要用于治疗先期化疗失败的晚期或转移性乳腺癌、以顺铂为主的化疗失败的晚期或转移性非小细胞肺癌。由法国Sanofi-Aventis开发,最早于1995年11月在欧盟上市。1996年5月FDA批准上市,2002年恒瑞医药该药品获批在国内上市,据悉,恒瑞医药是第九家获批上市的仿制药公司。
据药智国产药品数据库显示,目前国产多西他赛注射液生产批文有39条,生产企业20家,另据药智药品注册与受理数据库统计,截止目前申报一致性评价的有仅正大天晴和江苏恒瑞,值得注意的是正大天晴的该品种审评状态已于9月更新为“已发件”,却一直没有消息通告已过评,此次恒瑞也审评审批完毕,会否过评,值得关注的。
多西他赛注射液一致性评价详情表

盐酸伊立替康注射液
12月10日,据药智药品注册与受理数据库显示,江苏恒瑞医药的盐酸伊立替康注射液又一受理号一致性评价“审批完毕-待制证”。
盐酸伊立替康注射液是抗消化道肿瘤的化疗用药。原研公司为澳大利亚Pfizer(Perth)PtyLimited。据悉,目前国内盐酸伊立替康注射液市场主要由恒瑞,辉瑞及齐鲁制药占据,其中恒瑞占比超60%。
据药智国产药品数据库显示,我国现有盐酸伊立替康注射液国产批文9条,生产单位5家。目前申报一致性评价的企业仅齐鲁和恒瑞制药,此前齐鲁制药其中的2个受理号已发批件,恒瑞的一个受理号显示已发批件,如今又一受理号也已审批完毕,两家企业谁将拔得头筹,坐等官宣。
盐酸伊立替康注射液一致性评价详情表
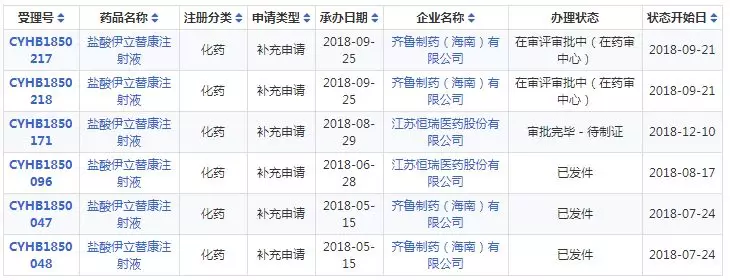
草酸艾司西酞普兰片
12月10日,据药智药品注册与受理数据库显示,浙江金华康恩贝生物制药草酸艾司西酞普兰片“审批完毕-待制证”。
据药智药品注册与受理数据库显示,截止目前,草酸艾司西酞普兰片一致性评价申报企业4家,其中四川科伦药业、湖南洞庭药业和山东京卫制药3家企业已经相继过评,此次,若浙江金华康恩贝生物制药该药品顺利通过将成为第4家过评企业。
草酸艾司西酞普兰片一致性评价详情表
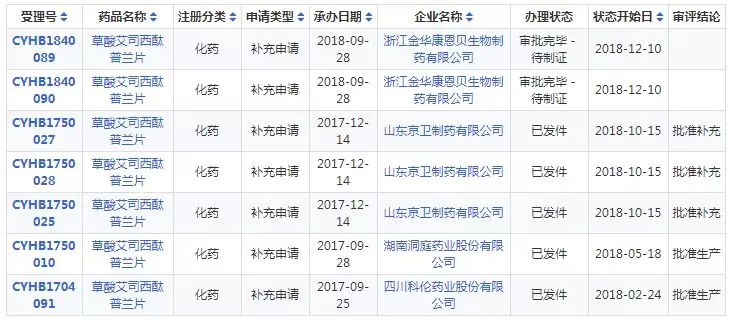
一致性评价承办状态更新
本周CDE新增一致性评价受理号36个,涉及23个品种,其中289目录药品16个受理号(12品种);还有5个注射剂申报一致性评价获受理,其中3个为首家申报,为齐鲁制药盐酸格拉司琼注射液、本溪恒康制药的醋酸奥曲肽注射液和烟台东诚北方制药的注射用那屈肝素钙;另外,东北制药集团沈阳第一制药齐多夫定片,烟台万润药业的诺氟沙星胶囊,苏州中化药品工业的头孢克洛胶囊,西南药业的盐酸吗啡缓释片也为首家申报获受理品种,因此本周共有7个首家申报药品。以下看看其中几个药品情况:
本周一致性评价申报获受理详情表
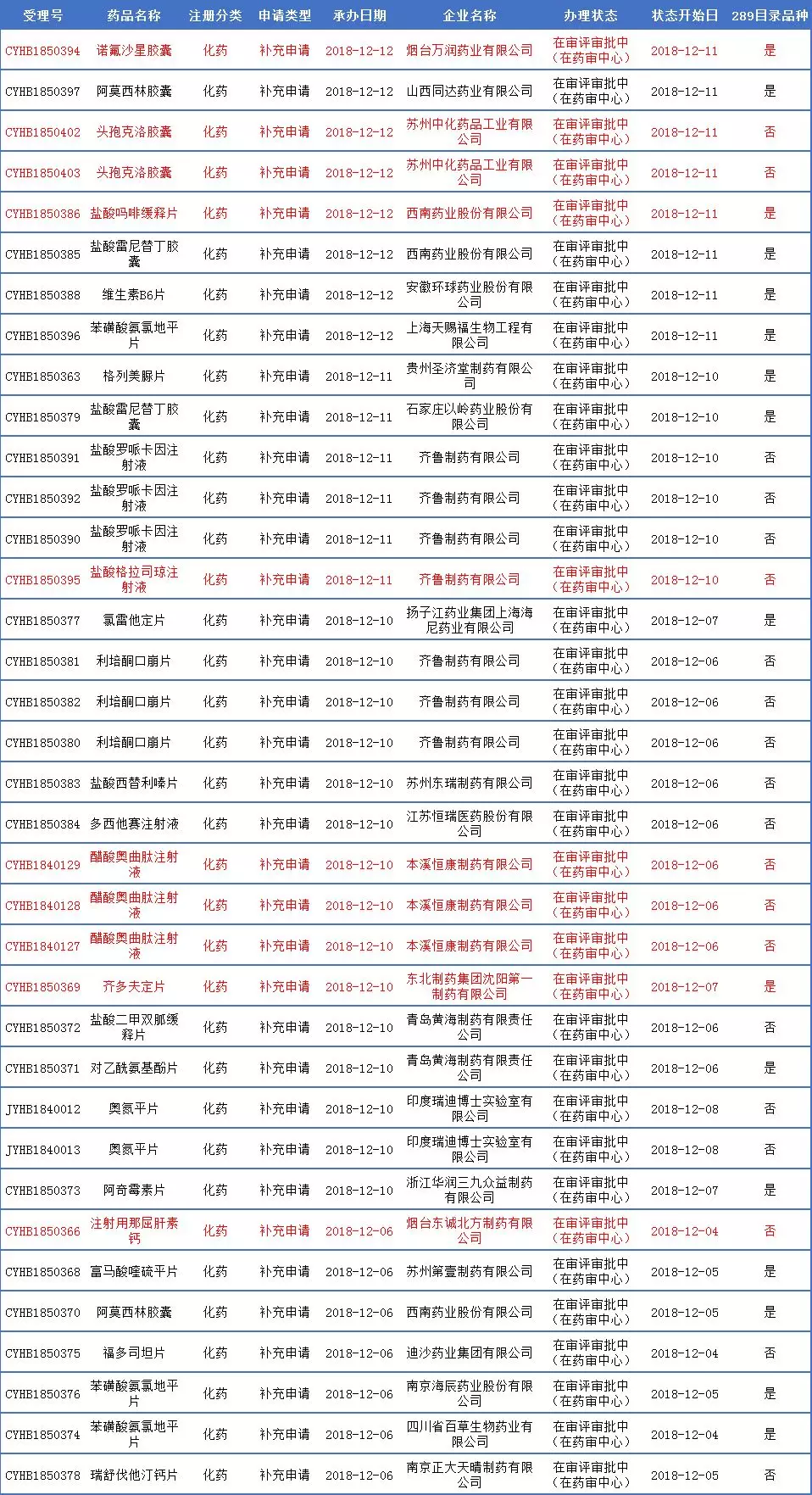
盐酸格拉司琼注射液
12月10日,齐鲁制药盐酸格拉司琼注射液一致性评价获CDE承办。
盐酸格拉司琼注射液第一代5-HT3受体拮抗剂,用于放射治疗、细胞毒类药物化疗引起的恶心和呕吐。由罗氏原研,据药智数据显示,现有国产盐酸格拉司琼注射液国产批文40条,生产企业34家,申报一致性评价目前仅齐鲁制药,亦没有其他企业参比备案。
醋酸奥曲肽注射液
12月10日,本溪恒康制药醋酸奥曲肽注射液一致性评价获CDE承办。
醋酸奥曲肽注射液是人工合成的八肽化合物,为十四肽人生长抑素类似物,国家乙类医保目录药品,临床主要用于治疗胰腺炎、食管-胃静脉曲张出血、防治胃肠胰瘘等症状。奥曲肽是由化学家WilfriedBauer于1979年首次合成。原研单位为诺华制药,作用靶点是GHRF,SSTR。1988年获批上市,商品名为善宁。
据药智数据显示,我国现有醋酸奥曲肽注射液国产批文28条,生产企业16家,申报该药品一致性评价的企业仅本溪恒康制药,国药一心制药和上海诺华贸易有进行参比备案。
注射用那屈肝素钙
12月6日,烟台东诚北方制药的注射用那屈肝素钙一致性评价获CDE承办。
那屈肝素钙是一种新型的抗血栓形成药物,通过解聚从猪肠黏膜中提取的肝素而得,属于低分子肝素制剂。原研企业为葛兰素史克的速碧林。据悉那屈肝素是全球销量最大的3种低分子肝素制剂之一,全球销售额超过3亿美元。国内那曲肝素钙制剂(含低分子肝素钙)市场模约20亿元,速碧林占据近半市场份额。
据药智国产数据库显示,注射用那屈肝素钙目前仅烟台东诚北方制药拥有国产批文,是国内拥有的唯一那屈肝素钙粉针剂型,且由于国家已经停止该剂型那屈肝素钙的审批,所以烟台东诚北方制药将是永久独家。此次申报一致性评价若顺利过评,将更加巩固其市场地位,并向原研发起冲击。
齐多夫定片
12月10日,东北制药集团沈阳第一制药289目录药品齐多夫定片一致性评价申报获CDE承办。
齐多夫定为抗病毒药,用于艾滋病或与艾滋病有关的综合症患者及免疫缺陷病毒(HIV)感染的治疗。由葛兰素史克原研,1987年获FDA批准上市,其是世界上第一个获得美国FDA批准生产的抗艾滋病药品,因其疗效确切,成为“鸡尾酒”疗法最基本的组合成分。
据药智国产数据库显示,我国现有齐多夫定片国产批文8条,生产企业6家,另据药智药品一致性评价进度数据库,上海迪赛诺生物医药已参比备案一致性评价,东北制药集团沈阳第一制药首家申报获受理,值得一提的是该品种可豁免BE试验,有望加速过评。
声明:本文观点仅代表作者本人,不代表药智网立场,欢迎在留言区交流补充;如需转载,请务必注明文章作者和来源。
文来自:药智汇